Закон термодинамики первый — один из фундаментальных законов физики, который формулирует основные положения и принципы о тепловых явлениях. Согласно этому закону, всякая тепловая система термодинамическое равновесие достигает при одинаковой температуре всех ее частей.
Первый закон термодинамики также известен как закон сохранения энергии в теплотехнике. В соответствии с этим законом, тепло и работа являются формами энергии, а все тепловые явления и рабочие процессы основаны на примерно тех же принципах. Установлено, что количество работы, совершенной в тепловых циклах термодинамических машин, пропорционально количеству тепла, которое выделилось или поглощено этими машинами.
В основе первого закона термодинамики лежат понятия энергии внутренней и внешней. Внутренняя энергия системы зависит только от ее состояния и определяется идеальным газовым законом. Внешняя энергия — это работа, выполняемая системой или полностью, или отчасти. Обобщенные положения первого закона существенны для понимания работы и энергии в целом и имеют большое значение в нашей повседневной жизни и промышленности.
Термодинамика первого закона: основные положения и принципы
Основные положения термодинамики первого закона следующие:
1. Внутренняя энергия системы. Внутренняя энергия системы – это сумма всей энергии, находящейся внутри системы, включая кинетическую и потенциальную энергию всех ее частиц. Изменение внутренней энергии системы зависит от количества тепла, переданного или поглощенного системой, а также от работы, совершенной над системой или совершенной ею.
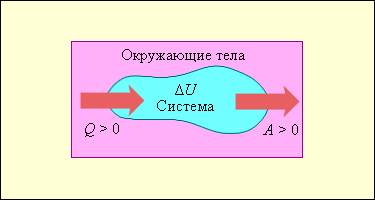
2. Количество тепла и работы. Первый закон термодинамики гласит, что изменение внутренней энергии системы равно сумме количества тепла, переданного или поглощенного системой, и работы, совершенной над системой или совершенной ею. Количество тепла и работы являются формами энергии, которые могут быть переданы между системой и окружающей средой.
3. Закрытая система и работа. В закрытой системе количество тепла, потери и доходы делают работу. Работа может быть совершена над системой или системой. При выполнении работы система теряет или получает энергию. Работа может менять состояние системы, увеличивая или уменьшая ее внутреннюю энергию.
4. Уравнение первого закона. Уравнение первого закона термодинамики устанавливает равенство: изменение внутренней энергии системы равно сумме количества тепла и работы. В математической форме это выглядит следующим образом: ΔU = Q — W, где ΔU – изменение внутренней энергии системы, Q – количество тепла, W – работа, совершенная над или совершенная системой.
Термодинамика первого закона является основополагающей для изучения тепловых процессов и многих других областей физики. Понимание основных положений и принципов термодинамики первого закона позволяет рассматривать энергию как физическую величину, которая сохраняется в системе, и более точно анализировать тепловые явления и процессы.
Роль термодинамики первого закона в естественных науках
В естественных науках, включая физику, химию, астрономию и биологию, термодинамика первого закона используется для объяснения и предсказания различных явлений и процессов.
- Физика: Термодинамика первого закона позволяет описывать и изучать тепловые явления, включая теплопередачу, тепловое расширение и изменение внутренней энергии системы. Этот закон также применим для решения задач, связанных с изменением состояния вещества и переходом тепловой энергии в другие виды энергии.
- Химия: В химических реакциях термодинамика первого закона позволяет определить изменение энергии системы и ее окружения. Этот закон помогает понять, какие реакции являются экзотермическими (выделяющими тепло) или эндотермическими (поглощающими тепло), а также предсказать условия, при которых реакции могут происходить или прекращаться.
- Астрономия: В астрономии термодинамика первого закона играет ключевую роль в изучении звезд и галактик. Этот закон позволяет ученым определить, как энергия возникает и распространяется в этих системах, а также предсказать их эволюцию и конечное состояние.
- Биология: Также термодинамика первого закона имеет важное значение в биологии. Он позволяет понять, как энергия переходит через жизненные системы, включая растения и животные. Этот закон помогает изучать обмен энергией в организме, его возможности для работы и возможное потребление и выделение тепла.
Таким образом, термодинамика первого закона играет неотъемлемую роль в естественных науках, обеспечивая понимание и объяснение энергетических процессов и явлений. Она является основой для развития других отраслей науки и помогает в разработке новых технологий и улучшении нашего понимания окружающего нас мира.
Законы термодинамики и их значение
Первый закон термодинамики — также известный как закон сохранения энергии. Он утверждает, что внутренняя энергия системы может меняться, но сумма изменения внутренней энергии и работы, совершенной над системой, равна внешнему теплоте, переданному системе.
Второй закон термодинамики — говорит о направлении тепловых процессов. Он утверждает, что теплота сама по себе не может переходить из холодного тела в горячее. Она всегда переходит от тела с более высокой температурой к телу с более низкой температурой. Второй закон также вводит понятие энтропии — меры беспорядка или неупорядоченности системы.
Третий закон термодинамики — устанавливает невозможность достижения абсолютного нуля температуры. Он утверждает, что при достижении абсолютного нуля все молекулярные движения и колебания в системе прекращаются. Этот закон имеет важное значение для понимания свойств и поведения вещества при очень низких температурах.
Законы термодинамики являются основой для различных инженерных и научных применений, например, в области энергетики и технологии производства. Они помогают предсказывать и оптимизировать эффективность систем, а также разрабатывать новые материалы и процессы.
Определение термодинамики первого закона
Термодинамический первый закон устанавливает равенство между изменением внутренней энергии системы и суммой работы, выполненной над системой и переданной ей калорий. Это означает, что изменение энергии системы равно разности между количеством тепла, полученным системой, и количеством работы, совершенной над системой.
Термодинамика первого закона имеет широкое применение в различных областях науки и техники, включая инженерию, физику, химию и геологию. Она позволяет анализировать тепловые процессы и определять их эффективность, а также рассматривать равновесные и необратимые процессы. Этот закон является базовым принципом в термодинамике и служит фундаментом для разработки более сложных принципов и законов в этой области науки.
Основные принципы термодинамики первого закона
Основные принципы этого закона заключаются в следующем:
1. Принцип сохранения энергии
Согласно первому принципу термодинамики, энергия не может быть создана или уничтожена, только преобразована из одной формы в другую. Это означает, что полная энергия замкнутой системы остается постоянной во время всех процессов теплообмена и работы.
2. Принцип работы
Принцип работы заключается в том, что совокупная работа, совершенная на замкнутой системе, равна изменению полной энергии системы. Если система получает тепло и выполняет работу, то энергия системы увеличивается на величину полученного тепла плюс совершенную работу.
3. Принцип теплообмена
Принцип теплообмена устанавливает, что тепло может переходить от системы с более высокой температурой к системе с более низкой температурой. Разность температур между системами определяет направление потока тепла.
Основные принципы термодинамики первого закона лежат в основе различных термодинамических процессов, позволяют оценить работу и энергетическую эффективность систем, и являются фундаментом для развития более сложных законов и принципов термодинамики.
Принцип сохранения энергии
Этот принцип можно представить в виде уравнения:
Энергия до = Энергия после
То есть, сумма энергий всех систем в изолированной системе остается постоянной со временем.
Примеры применения принципа сохранения энергии можно найти в различных областях. Например, в механике. Когда тело движется под действием силы, его кинетическая энергия увеличивается, но при этом потенциальная энергия уменьшается на такую же величину, чтобы сохранить общую энергию системы неизменной.
Принцип сохранения энергии имеет фундаментальное значение не только для термодинамики, но и для различных научных и инженерных задач. Он позволяет определить энергетические потоки и взаимодействия, а также разрабатывать эффективные системы энергетики и устройства, основанные на превращении энергии из одной формы в другую.
Процессы равновесия и неравновесия
Процесс равновесия подразумевает состояние системы, в котором все физические процессы происходят без изменения или с минимальными изменениями. В равновесном состоянии все макроскопические свойства системы остаются постоянными во времени и пространстве. Процессы равновесия являются предельными состояниями, которые система стремится достичь.
Процесс неравновесия представляет собой отличие от состояния равновесия, когда система находится в постоянном изменении. В неравновесных процессах происходят перераспределение энергии, массы и других физических величин в системе. Эти процессы являются неустойчивыми и не могут продолжаться бесконечно.
Процессы равновесия и неравновесия являются важными для понимания и описания физических процессов. Изучение этих процессов позволяет определить, как система достигает равновесия и каким образом она может переходить из состояния равновесия в неравновесие и наоборот.
Зависимость энергии от состояния системы
Важно подчеркнуть, что энергия системы — внутренняя характеристика системы, которая может изменяться при взаимодействии с окружающей средой. Однако, вне зависимости от внешних воздействий, энергия системы всегда будет определяться ее состоянием.
Знание об этой зависимости важно для понимания работы термодинамических систем и проведения расчетов. Оно позволяет определить энергию системы, не зная историю ее изменений, а также сравнивать энергию разных систем в одном и том же состоянии.
Таким образом, понимание зависимости энергии от состояния системы является ключевым принципом, который лежит в основе термодинамических расчетов и позволяет установить единый подход к анализу и описанию различных физических систем.
Примеры применения термодинамики первого закона
1. Тепловые двигатели: Термодинамика первого закона широко применяется в изучении и проектировании тепловых двигателей, таких как паровые и газовые турбины, двигатели внутреннего сгорания и другие. Закон позволяет определить эффективность работы двигателя, а также его мощность и энергетические потери.
2. Отопление и охлаждение: В системах отопления и кондиционирования воздуха также используются принципы термодинамики первого закона. Закон позволяет определить необходимую мощность системы для поддержания заданной температуры, а также энергетические потери и эффективность системы.
3. Процессы сжатия и расширения газов: При сжатии или расширении газов закон сохранения энергии, включая работу и теплоту, позволяет определить изменение внутренней энергии газа и его температуры. Это, в свою очередь, имеет множество применений в промышленности, научных исследованиях и технике.
4. Процессы смешивания и разделения веществ: Термодинамика первого закона также применяется для анализа процессов смешивания и разделения веществ. Закон позволяет определить изменение энергии при смешении различных веществ или их разделении на составляющие части.
5. Энергетические системы: В энергетических системах, таких как электростанции и сети передачи электроэнергии, закон сохранения энергии является основополагающим. Закон применяется для определения энергетических потерь, оптимизации работы системы и повышения эффективности процессов передачи и преобразования энергии.
6. Химические реакции: Принципы термодинамики первого закона применяются для изучения и анализа химических реакций, включая определение энергетических потерь или выделения тепла, изменения внутренней энергии и энтальпии веществ.
Примеры применения термодинамики первого закона охватывают широкий спектр областей, от механических систем и энергетики до химических и биологических процессов. Закон сохранения энергии является одной из основных принципов в науке и находит применение во многих практических ситуациях.
Вопрос-ответ:
Что такое закон термодинамики?
Закон термодинамики — основной закон физики, который описывает закономерности процессов, происходящих в системах, связанных с тепловым движением частиц. Весьма объемным есть так, что есть 4 закона термодинамики, но первый закон термодинамики описывает сохранение энергии в системе и гласит, что энергия не может быть создана или уничтожена, она только может преобразовываться из одной формы в другую.
Какие принципы лежат в основе первого закона термодинамики?
В основе первого закона термодинамики лежат два принципа: принцип сохранения энергии и принцип неразделимости системы с окружающей средой. Принцип сохранения энергии утверждает, что энергия не может быть создана или уничтожена, она только может преобразовываться из одной формы в другую. Принцип неразделимости системы с окружающей средой означает, что энергия может переходить между системой и окружающей средой, но их суммарная энергия остается постоянной.
Какие типы систем описывает закон термодинамики?
Закон термодинамики описывает закономерности процессов, происходящих в различных типах систем. Системы могут быть открытыми, закрытыми или изолированными. В открытой системе энергия и вещество могут свободно переходить через ее границы с окружающей средой. В закрытой системе энергия может переходить, но вещество — нет. В изолированной системе ни энергия, ни вещество не могут переходить через ее границы.
Как применяется закон термодинамики в реальной жизни?
Закон термодинамики применяется во многих сферах жизни. Например, он используется при разработке энергетических систем, чтобы рассчитать и оптимизировать эффективность работы тепловых двигателей. Он также применяется в химической промышленности для контроля химических реакций и определения эффективности производства. В медицинских приборах, таких как МРТ и ультразвуковые сканеры, закон термодинамики используется для создания и контроля тепловой энергии.